¿Primitivos autómatas celulares?
Artículo original de André Brack, exobiólogo. Autora de la traducción: Marisa Raich
La unidad del ser vivo contemporáneo y su modo de funcionamiento celular sugiere que la vida apareció con los rasgos de una célula simplificada.
Durante decenios, los químicos se han esforzado por reconstituir en el laboratorio las moléculas indispensables para el funcionamiento de una célula contemporánea: las moléculas de compartimentación, las moléculas catalíticas y las moléculas de información (plano de montaje).
1 - Las membranas primitivas.
Las membranas garantizan la cohesión de la célula. Están formadas por moléculas anfífilas que poseen a la vez una cabeza polar hidrófila y cadenas carbonadas hidrófobas. Los ácidos grasos forman vesículas a condición de que la cadena hidrocarbonada encierre al menos diez átomos de carbono. No obstante, las membranas obtenidas con ayuda de estos compuestos anfífilos simples sólo son estables en una estrecha gama de condiciones experimentales, de manera que muy probablemente fueron necesarios compuestos químicos más complejos para conferir una buena estabilidad a las membranas primitivas. Los oligómeros cortos del isopreno representan una pista interesante. Sus derivados entran en la composición de ciertas vitaminas (E o K1, por ejemplo) y de la clorofila, pero sobre todo en la de los lípidos de ciertas archaea (halobacterium cutirubrum, por ejemplo). En Estrasburgo, el equipo del químico francés Guy Ourisson obtuvo vesículas fijando dos cadenas de diisopreno sobre un grupo fosfatado. El análisis de meteoritos carbonados permitió detectar la presencia de ácidos grasos de ocho átomos de carbono en los extractos del meteorito de Murchison. Ciertas sustancias orgánicas extraídas de las condritas carbonadas de Murchison y de Allende forman, en medio acuoso, estructuras compartimentadas parecidas a membranas.
2 - Las mini-proteínas.
En una célula contemporánea, la copia de la información química está garantizada por proteínas químicamente activas, las enzimas. Los 20 ácidos α-aminados utilizados por las enzimas, del tipo NH2-CHR-COOH, constan de una función amino NH2 y una función ácida COOH separadas por un único átomo de carbono. Se diferencian por la naturaleza del sustituto R. Éste presenta a veces una función químicamente activa, sede de la actividad catalítica. Los ácidos α-aminados con diversos átomos de carbono entre las funciones amino y ácida y los ácidos aminados disustituídos que presentan dos sustituyentes carbonados en el átomo de carbono central no se utilizan. Se forma una cadena peptídica por la eliminación de una molécula de agua entre las funciones amino y ácidas carboxílicas de los ácidos aminados. La química de los péptidos ofrece toda una panoplia de reacciones que permiten condensar los ácidos aminados en los disolventes orgánicos. En el agua, el número de estos métodos es mucho más limitado, sobre todo cuando sólo se registran las reacciones que pudieran estar presentes en la Tierra primitiva. Según Christian de Duve, los primeros péptidos se formaron mediante los tioésteres, (N. Del T.ésteres que tienen un átomo de oxigeno sustituido por un átomo de azufre), que permiten generar péptidos cortos en presencia de superficies minerales. Los derivados activados de los ácidos aminados más activos en el agua son probablemente los N-carboxianhídridos. El calor solo también permite condensar los ácidos aminados. Investigadores japoneses hicieron pasar en circuito cerrado una solución de glicina y de cloruro de cobre desde una cámara de reacción preparada a 220ºC y 200 atmósferas a una cámara mantenida a 0ºC y 200 atmósferas para imitar las condiciones de baño térmico que reinan en la proximidad de las fuentes cálidas submarinas. Consiguieron así polimerizar la glicina hasta el grado del octámero. A 220ºC en ausencia de baño térmico, sólo se observa la descomposición química del ácido aminado.
En nuestro equipo de Orleáns demostramos que el agua, por sus propiedades químicas, orienta la reacción de polimerización y permite la selección de los ácidos aminados proteicos. Las proteínas adoptan esencialmente dos geometrías rígidas, la hélice α y las láminas β. Las hélices α se obtienen fácilmente: basta con tomar un ácido aminado hidrófilo (soluble en agua dado que presenta una función ionizable en la cadena lateral) y un ácido aminado hidrófobo (muy poco soluble en agua) y ligarlos entre sí sin preocuparse por el orden de encadenamiento. Cuando las cadenas son lo bastante largas, de una veintena de ácidos aminados aproximadamente, adoptan en el agua la configuración de hélice α. Por el contrario, todos los polipéptidos construidos sobre una alternancia estricta de ácidos aminados hidrófilos e hidrófobos adoptan una estructura de lámina β en el agua por agregación de los grupos hidrófobos. Al añadir alcohol al agua, la fuerza de las interacciones hidrófobas que genera las láminas β se atenúa y el polipéptido adopta entonces una configuración helicoidal α. Por lo tanto, es el agua la que, por sus propiedades físicas específicas, permite la estructuración en láminas β. Los polipéptidos de secuencia alternada, capaces por ello de adoptar la geometría β, presentan una buena estabilidad química. En las mismas condiciones experimentales, las cadenas que encierran los mismos ácidos aminados enlazados en desorden se degradan con mucha más facilidad. En consecuencia, la degradación es selectiva. Podría haber permitido la selección de secuencias alternas, más resistentes, contribuyendo así a restringir la complejidad química en el curso de la evolución. La formación de láminas β requiere la utilización de ácidos aminados de la misma configuración, todos L o todos D. Cuando las secuencias alternadas encierran a la vez enantiómeros L y D distribuidos al azar a lo largo de las cadenas, únicamente los segmentos que contienen al menos seis ácidos aminados L (o D) consecutivos de agregan en islotes β, ópticamente puros (Brack, 1980). Numerosos péptidos cortos y ciertos polipéptidos simples manifiestan una actividad catalítica, es decir que son capaces de acelerar ciertas reacciones químicas. Por ejemplo, demostramos que los péptidos básicos cortos que sólo encierran dos ácidos aminados distintos cortan los ácidos ribonucleicos.
3 - Los mini-ARN.
Los ácidos nucleicos actuales contienen información genética que permite la formación de una célula-hija idéntica a la célula-madre. Se trata de cadenas muy largas constituidas por la repetición de nucleótidos. Cada nucleótido se compone de un azúcar (ribosa dotada de un grupo OH en el caso del ARN, desoxiribosa en el ADN), de una base (purina A, G o pirimidina T, U, C) y de un grupo fosfatado. (Figura 2).
Figura 2. Cada nucleótido se compone de un grupo fosfatado, de un azúcar y de una base heterocíclica.
El establecimiento de enlaces hidrogenados permite el emparejamiento preferencial de las bases. Gracias al emparejamiento de las bases, el ADN adopta una configuración estable en doble hélice constituida por la asociación capiculada de dos hebras polinucleotídicas complementarias. El emparejamiento de las bases proporciona también al ADN el medio para transferir la información que lleva impresa en su secuencia mediante un mecanismo de auto-replicación: las dos hebras complementarias se separan y cada una de ellas sirve de matriz para la síntesis de una nueva cadena. La copia se realiza con una excelente precisión dado que la tasa de error de traducción es del orden de un ácido aminado de cada diez mil.
La gran mayoría de trabajos de reconstitución en laboratorio de ácidos nucleicos prebióticos se refiere a los ácidos nucleicos de ribosa (ARN) dado que se les considera más antiguos, más primitivos, que los ADN de desoxiribosa. El fósforo está presente en las rocas ígneas terrestres en forma de fluoroapatita (un fluorofosfato de calcio) que representa un 0,6% de la masa mineral total. La cloroapatita es el fosfato mineral más abundante en los meteoritos. La fluoroapatita prácticamente no es soluble en agua a pH 7, pero se puede aumentar fuertemente la solubilidad mediante complejación con un diácido como, por ejemplo, el ácido oxálico. Las bases púricas se obtienen fácilmente a partir del ácido cianhídrico, o bien sometiendo a descargas eléctricas una mezcla gaseosa de metano, etano y amoníaco. No obstante, los rendimientos de síntesis son muy débiles. Las bases púricas y pirimídicas están presentes en los meteoritos y posiblemente en los cometas. La síntesis de los azúcares a partir de formaldehído proporciona una mezcla muy compleja en la cual el azúcar buscado es muy minoritario. La síntesis de nucleósidos, asociación de una base y ribosa, puede realizarse mediante simple calentamiento en estado sólido. Los rendimientos, no obstante, son muy débiles. Además, la base se enlaza en varios puntos del azúcar, sin una preferencia marcada por el enlace natural. La fijación del grupo fosfato al nucleósido se puede obtener también mediante calentamiento. El grupo fosfato se fija a la ribosa pero, también en este caso, sin ninguna especificidad. La formación de una cadena de ácido nucleico requiere la eliminación de una molécula de agua entre el grupo fosfato y el azúcar.
El químico americano James Ferris descubrió una arcilla que cataliza eficazmente la condensación de los nucleótidos. La síntesis de oligómeros de ARN es eficaz en presencia de una hebra de ARN preformada que sirve de matriz. La replicación química, o no enzimática, ha sido estudiada con éxito por Leslie Orge. Las hebras preformadas de poli C (un poliribonucleótido de pirimidinas) son capaces de seleccionar los nucleótidos complementarios G (de purinas) para formar una doble hélice gracias al emparejamiento de las bases G...C. La estructura helicoidal alinea los nucleótidos G a lo largo de Poli C e induce a los grupos reactivos en contacto, lo cual les permite reaccionar. La reacción de condensación es muy eficaz y conduce a la formación de enlaces naturales 3'-5'. La reacción es altamente específica porque sólo se incorpora el nucleótido activado G complementario de la matriz poli C. Si se presenta a la matriz un cóctel de nucleótidos, el nucleótido complementario se incorpora de 100 a 500 veces más eficazmente. En ausencia de matriz, la condensación de G activado es muy poco eficaz y conduce a una mezcla compleja de productos de pequeña talla. También es posible transferir la información de secuencia a la matriz. La secuencia matricial C-C-G-C-C dirige la condensación de una mezcla de G y de C activados y produce G-G-C-G-G preferencialmente a las otras secuencias. No obstante, la síntesis sobre matriz tropieza todavía con cierto número de dificultades. Por ejemplo, en los experimentos de replicación química, la matriz está constituida por azúcares D y los nucleótidos activados también son D. Alimentando la matriz D con nucleótidos L, la condensación es poco eficaz. Al utilizar una mezcla racémica que contenga tantos nucleótidos D como nucleótidos L, se observa una inhibición casi total de la reacción dado que los nucleótidos L envenenan la condensación de los nucleótidos D. La replicación química sólo se desarrolla con moléculas ya seleccionadas, situación poco plausible en la Tierra primitiva.
Los químicos buscaron entonces sacar provecho de análogos de los ácidos nucleicos biológicos. Unos notables trabajos del químico suizo Albert Eschenmoser centrados en el posible papel del fosfato de glicoaldehído en la evolución química demuestran que este compuesto conduce fácilmente en presencia de formaldehído a un azúcar ribopiranoso, es decir, un ciclo oxigenado de 6 átomos. Los estudios, todavía no finalizados, ya han dado resultados prometedores (Eschenmoser, 1999). La síntesis de un análogo de ARN construido sobre la forma furanósila de la triosa (una tetrosa) también ha sido descrita por el grupo de Eschenmoser (Schöning et al., 2000). Los ácidos nucleicos péptidos, sintetizados inicialmente por Nielsen y sus colaboradores (Koppitz et al., 1998), comportan un esqueleto aquiral de poli-2-aminoetil glicina. No obstante, la formación prebiótica de ARN continúa inexplicada.
Para saber más:
La Anfifila, es una estructura molecular con una sección polar y otra apolar, lo que le permite asociarse con un amplio rango de materiales. Del griego Anfifila es "amigo de dos cosas"; esto proviene de que su estructura consta de dos partes: una hidrófila y otra hidrófuga. Esta estructura hace que en presencia de agua, las anfifilas adopten su estructura de micela. Las anfífilas ayudan a la fragmentación de polímeros para dar coroides. También forman parte de membranas celulares semipermeables para permitir la regulación de ciertos aspectos biológicos ( la presión osmótica por ejemplo ).
Los péptidos son un tipo de moléculas formadas por la unión de varios aminoácidos mediante enlaces peptídicos. Los péptidos, al igual que las proteínas, están presentes en la naturaleza y son responsables de un gran número de funciones, muchas de las cuales todavía no se conocen. La unión de un bajo número de aminoácidos da lugar a un péptido:
Se dice que una molécula constituye un oligómero cuando los radicales asociados son distintos entre sí. La naturaleza orgánica esta llena de estos casos multifuncionales. En cambio, un polímero es una molécula con dos o más radicales de la misma especie. Un grupo de 3 a 9 moléculas de monómero que se han unido entre sí para formar una molécula más grande. Pueden ser dímeros, trímeros, tetrámeros, pentámeros, etc.
Las bases nitrogenadas son compuestos orgánicos cíclicos, que incluyen dos o más átomos de nitrógeno. Son parte fundamental de los nucleósidos, nucleótidos y ácidos nucleicos. Biológicamente existen cinco bases nitrogenadas principales, que se clasifican en dos grupos, bases púricas (derivadas de la estructura de la purina) y bases pirimidínicas (derivadas de la estructura de la pirimidina). La adenina (A) y la guanina (G) son púricas, mientras que la timina (T), la citosina (C) y el uracilo (U) son pirimidínicas. Las cuatro primeras bases se encuentran en el ADN, mientras que en el ARN en lugar de timina existe el uracilo.
La purina es una base nitrogenada, un compuesto orgánico heterociclíco. Dos de las bases de los ácidos nucleicos, adenina (también llamada 6-aminopurina) y guanina (o 2-amino-6-purina), son derivados de la purina. En el ADN (ácido desoxirribonucleico, almacenador principal y fundamental de la información genética en todos los seres vivos), estas bases se unen con sus pirimidinas complementarias, la timina (2,6-dioxi-5-metilpirimidina) y la citosina (2-oxi-6-aminopirimidina), a través de enlaces de hidrógeno.
Traducido y editado por el equipo de Astroseti.
Colaboradores:
- Marisa Raich
- Xavier CivitPróximo capítulo:
- ¿Una vida primitiva más simple que la célula?.Capítulos ya publicados de la misma serie:
Crédito de las imágenes: NASA, Futura-Sciences.
- La exobiología: del origen de la vida a la vida en el Universo (I)
- La exobiología: del origen de la vida a la vida en el Universo (II): Las diferentes fuentes de moléculas orgánicas, un origen terrestre
- La exobiología: del origen de la vida a la vida en el Universo (III): Las diferentes fuentes de moléculas orgánicas, las moléculas orgánicas extraterrestres
- La exobiología: del origen de la vida a la vida en el Universo (IV): Experimentos de simulación en laboratorio y en órbita terrestre
- La exobiología: del origen de la vida a la vida en el Universo (V): ¿Primitivos autómatas celulares?
- La exobiología: del origen de la vida a la vida en el Universo (VI): ¿Una vida primitiva más simple que la célula?
- La exobiología- Del origen de la vida a la vida en el Universo (VII): La búsqueda de autómatas fósiles
- La exobiología- Del origen de la vida a la vida en el Universo (VIII): A la busca de una vida extraterrestre, cómo evidencia de simplicidad.
- La exobiología- Del origen de la vida a la vida en el Universo (IX): Los Exoplanetas.
- La exobiología- Del origen de la vida a la vida en el Universo (y X): Clonclusión.Enlace original: http://www.futura-sciences.com/
Fuente: astroseti.org/


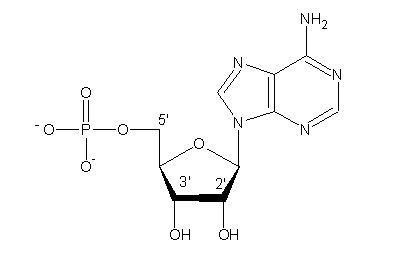




 Imagen actualizada por la USNO
Imagen actualizada por la USNO







0 comentarios:
Publicar un comentario
Todos los comentarios son responsabilidad únicamente de sus autores y no refleja necesariamente el punto de vista de este sitio.
NO insultes a nadie.